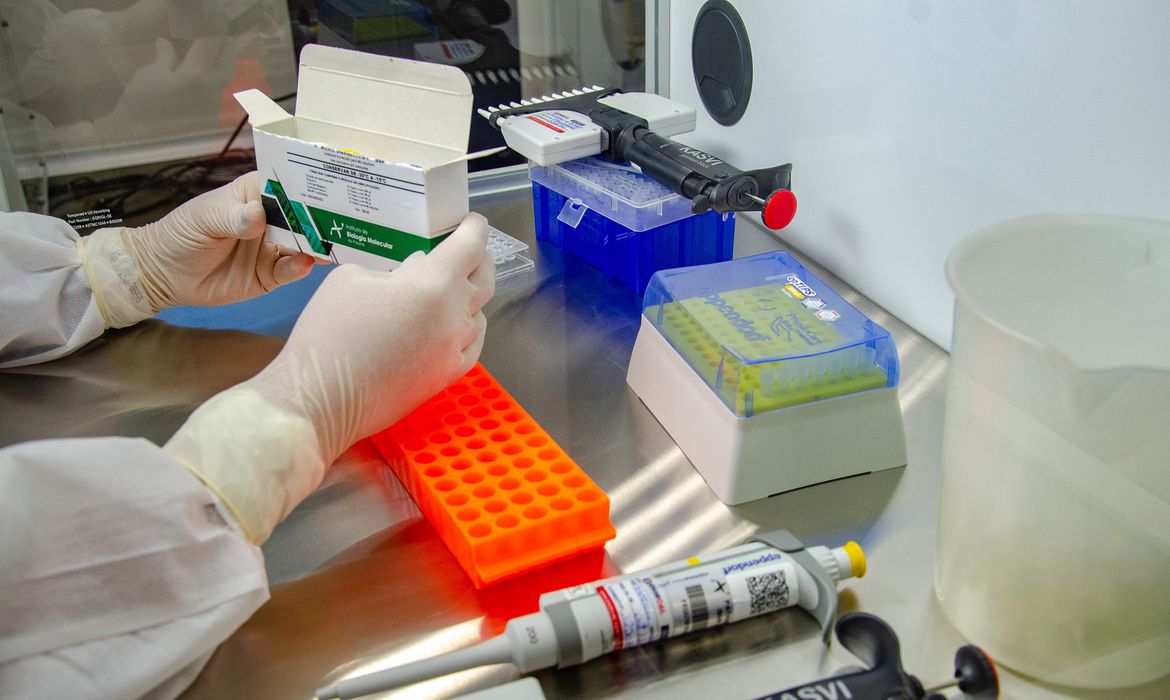
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a Jansen-Cilag, unidade farmacêutica da Johnson & Johnson, a realizar testes clínicos no Brasil para o desenvolvimento de vacina contra a covid-19.
[wp_bannerize_pro orderby=”random” categories=”wp-bannerize-plano-1″ numbers=”1″ mobile=“1”]
O estudo global prevê a inclusão de até 60 mil voluntários, sendo 7 mil no Brasil, distribuídos nos estados de São Paulo, Rio Grande do Sul, Rio de Janeiro, Paraná, Minas Gerais, Bahia e Rio Grande do Norte.

Em nota divulgada hoje (18), a Anvisa informou que os dados que embasaram a autorização incluíram estudos não clínicos com a vacina e dados não clínicos e clínicos acumulados de outras vacinas que utilizam a mesma modelagem. Os estudos da Jansen-Cilag foram iniciados em julho nos EUA e na Bélgica. De acordo com a agência, o ensaio clínico será conduzido em etapas e cada etapa só será iniciada se os resultados que estiverem disponíveis no momento forem satisfatórios.
[wp_bannerize_pro orderby=”random” categories=”wp-bannerize-plano-3″ numbers=”1″ mobile=“1”]
Este é o quarto estudo de vacina contra o novo coronavírus autorizado pela Anvisa no Brasil. No dia 2 de junho, a agência autorizou o ensaio clínico da vacina desenvolvida pela empresa AstraZeneca e pela Universidade de Oxford, do Reino Unido; no dia 3 de julho, o da vacina desenvolvida pela Sinovac Biotech, da China, em parceria com o Instituto Butantan; e no dia 21 de julho, o das vacinas desenvolvidas pela BioNTech, da Alemanha, e Wyeth/Pfizer, dos Estados Unidos.
A potencial vacina da Jansen-Cilag, denominada Ad26.COV2.S, é composta de um vetor recombinante, não replicante, de adenovírus tipo 26 (Ad26), construído para codificar a proteína S (Spike) do vírus Sars-CoV-2 (o novo coronavírus).
[wp_bannerize_pro orderby=”random” categories=”wp-bannerize-plano-4″ numbers=”2″ mobile=“1”]
O ensaio clínico aprovado é um estudo de fase 3, randomizado, duplo cego, controlado por placebo, para avaliar a eficácia e a segurança de Ad26.COV2.S na prevenção de covid-19 em adultos com 18 anos ou mais.
Cada participante receberá uma dose única da vacina ou placebo.
O recrutamento dos voluntários é de responsabilidade dos centros que conduzem a pesquisa.
[wp_bannerize_pro orderby=”random” categories=”wp-bannerize-plano-2″ numbers=”1″ mobile=“1”]
Agencia Brasil